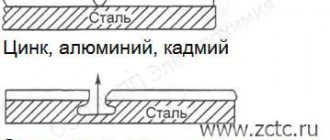
Цвет ржавчины
Ржавчина
— является общим термином для определения оксидов железа. В разговорной речи это слово применяется к красным оксидам, образующимся в ходе реакции железа с кислородом в присутствии воды или влажного воздуха. Есть и другие формы ржавчины, например, продукт, образующийся в ходе реакции железа с хлором при отсутствии кислорода. Такое вещество образуется, в частности, в арматуре, используемой в подводных бетонных столбах, и называют его
зелёной ржавчиной
. Несколько видов коррозии различимы зрительно или с помощью спектроскопии, они образуются при разных внешних условиях. Ржавчина состоит из гидратированного оксида железа (III) Fe2O3·nH2O и метагидроксида железа (FeO(OH), Fe(OH)3). При наличии кислорода, воды и достаточного времени любая масса железа в конечном итоге преобразуется полностью в ржавчину и разрушается. Поверхность ржавчины не создаёт защиту для нижележащего железа, в отличие от образования патины на медной поверхности.
Ржавчиной, как правило, называют продукт коррозии только железа и его сплавов, таких как сталь. Многие другие металлы тоже подвергаются коррозии, но именно оксиды железа обычно называют ржавчиной.
Химические реакции
Толстый слой ржавчины на звеньях цепи возле моста Золотые Ворота в Сан-Франциско. Цепь постоянно подвергается воздействию сырости и солёных брызг, вызывающих разрушение поверхности, растрескивание и шелушение металла.
Причины ржавления
Если железо, содержащее какие-либо добавки и примеси (например, углерод), находится в контакте с водой, кислородом или другим сильным окислителем и/или кислотой, то оно начинает ржаветь. Если при этом присутствует соль, например, имеется контакт с солёной водой, коррозия происходит быстрее в результате электрохимических реакций. Чистое железо относительно устойчиво к воздействию чистой воды и сухого кислорода. Как и у других металлов, например, у алюминия, плотно приставшее оксидное покрытие на железе (слой пассивации) защищает основную массу железа от дальнейшего окисления. Превращение же пассивирующего слоя оксида железа в ржавчину является результатом комбинированного действия двух реагентов, как правило, кислорода и воды. Другими разрушающими факторами являются диоксид серы и углекислый газ в воде. В этих агрессивных условиях образуются различные виды гидроксида железа. В отличие от оксидов железа, гидроксиды не защищают основную массу металла. Поскольку гидроксид формируется и отслаивается от поверхности, воздействию подвергается следующий слой железа, и процесс коррозии продолжается до тех пор, пока всё железо не будет уничтожено, или в системе закончится весь кислород, вода, диоксид углерода или диоксид серы.
Происходящие реакции
Покрытый ржавчиной и грязью болт. Заметна точечная коррозия и постепенная деформация поверхности, вызванная сильным окислением.
Ржавление железа — это электрохимический процесс, который начинается с переноса электронов от железа к кислороду. Скорость коррозии зависит от количества имеющейся воды, и ускоряется электролитами, о чём свидетельствуют последствия применения дорожной соли на коррозию автомобилей. Ключевой реакцией является восстановление кислорода:
O2 + 4 e− + 2 H2O → 4 OH−
Поскольку при этом образуются гидроксид-анионы, этот процесс сильно зависит от присутствия кислоты. Действительно, коррозия большинства металлов кислородом ускоряется при понижении pH. Обеспечение электронов для вышеприведённой реакции происходит при окисления железа, которое может быть описано следующим образом:
Fe → Fe2+ + 2 e−
Следующая окислительно-восстановительная реакция происходит в присутствии воды и имеет решающее значение для формирования ржавчины:
4 Fe2+ + O2 → 4 Fe3+ + 2 O2−
Кроме того, следующие многоступенчатые кислотно-щелочные реакции влияют на ход формирования ржавчины:
Fe2+ + 2 H2O ⇌ Fe(OH)2 + 2 H+ Fe3+ + 3 H2O ⇌ Fe(OH)3 + 3 H+
что приводит к следующим реакциям поддержания баланса дегидратации:
Fe(OH)2 ⇌ FeO + H2O Fe(OH)3 ⇌ FeO(OH) + H2O 2 FeO(OH) ⇌ Fe2O3 + H2O
Из приведённых выше уравнений видно, что формирование продуктов коррозии обусловлено наличием воды и кислорода. С ограничением растворённого кислорода на передний план выдвигаются железо (II)-содержащие материалы, в том числе FeO и чёрный магнит (Fe3O4). Высокая концентрация кислорода благоприятна для материалов с трёхвалентным железом, с номинальной формулой Fe(OH)3-xOx/2. Характер коррозии меняется со временем, отражая медленные скорости реакций твёрдых тел.
Кроме того, эти сложные процессы зависят от присутствия других ионов, таких как Ca2+, которые служат в качестве электролита, и таким образом, ускоряют образование ржавчины, или в сочетании с гидроксидами и оксидами железа образуют различные осадки вида Ca-Fe-O-OH.
Более того, цвет ржавчины можно использовать для проверки наличия ионов Fe2+, которые меняют цвет ржавчины с жёлтого на синий.
Газовая коррозия
Самая частая разновидность химической коррозии — газовая — представляет собой коррозийный процесс, происходящий в газах при повышенных температурах. Указанная проблема характерна для работы многих типов технологического оборудования и деталей (арматуры печей, двигателей, турбин и т.д.). Кроме того, сверхвысокие температуры используются при обработке металлов под высоким давлением (нагревание перед прокаткой, штамповкой, ковкой, термическими процессами и т.д.).
Особенности состояния металлов при повышенных температурах обуславливаются двумя их свойствами — жаропрочностью и жаростойкостью. Жаропрочность — это степень устойчивости механических свойств металла при сверхвысоких температурах. Под устойчивостью механических свойств понимается сохранение прочности в течение продолжительного времени и сопротивляемость ползучести. Жаростойкость — это устойчивость металла к коррозионной активности газов в условиях повышенных температур.
Скорость развития газовой коррозии обуславливается рядом показателей, в числе которых:
- температура атмосферы;
- компоненты, входящие в металл или сплав;
- параметры среды, где находятся газы;
- продолжительность контактирования с газовой средой;
- свойства коррозийных продуктов.
На коррозийный процесс больше влияние оказывают свойства и параметры оксидной пленки, появившейся на металлической поверхности. Образование окисла можно хронологически разделить на два этапа:
- адсорбция кислородных молекул на металлической поверхности, взаимодействующей с атмосферой;
- контактирование металлической поверхности с газом, в результате чего возникает химическое соединение.
Первый этап характеризуется появлением ионной связи, как следствие взаимодействия кислорода и поверхностных атомов, когда кислородный атом отбирает пару электроном у металла. Возникшая связь отличается исключительной силой — она больше, нежели связь кислорода с металлом в окисле.
Объяснение такой связи кроется в действии атомного поля на кислород. Как только поверхность металла наполняется окислителем (а это происходит очень быстро), в условиях низких температур, благодаря силе Ван-дер-Ваальса, начинается адсорбция окислительных молекул. Результат реакции — возникновение тончайшей мономолекулярной пленки, которая с течением времени становится толще, что усложняет доступ кислорода.
На втором этапе происходит химическая реакция, в ходе которой окислительный элемент среды отбирает у металла валентные электроны. Химическая коррозия — конечный результат реакции.
Характеристики оксидной пленки
Классификация оксидных пленок включает их три разновидности:
- тонкие (незаметны без специальных приборов);
- средние (цвета побежалости);
- толстые (видны невооруженным взглядом).
Появившаяся оксидная пленка имеет защитные возможности — она замедляет или даже полностью угнетает развитие химической коррозии. Также наличие оксидной пленки повышает жаростойкость металла.
Однако, действительно эффективная пленка должна отвечать ряду характеристик:
- быть не пористой;
- иметь сплошную структуру;
- обладать хорошими адгезивными свойствами;
- отличаться химической инертностью в отношении с атмосферой;
- быть твердой и устойчивой к износу.
Одно из указанных выше условий — сплошная структура имеет особенно важное значение. Условие сплошности — превышение объема молекул оксидной пленки над объемом атомов металла. Сплошность — это возможность окисла накрыть сплошным слоем всю металлическую поверхность. При несоблюдении этого условия, пленка не может считаться защитной. Однако, из этого правила имеются исключения: для некоторых металлов, например, для магния и элементов щелочно-земельной групп (исключая бериллий), сплошность не относится к критически важным показателям.
Чтобы установить толщину оксидной пленки, используются несколько методик. Защитные качества пленки можно выяснить в момент ее образования. Для этого изучаются скорость окисления металла, и параметры изменения скорости во времени.
Для уже сформированного окисла применяется другой метод, состоящий в исследовании толщины и защитных характеристик пленки. Для этого на поверхность накладывается реагент. Далее специалисты фиксируют время, которое понадобится на проникновение реагента, и на основании полученных данных делают вывод о толщине пленки.
Обратите внимание! Даже окончательно сформировавшаяся оксидная пленка продолжает взаимодействовать с окислительной средой и металлом.
Скорость развития коррозии
Интенсивность, с какой развивается химическая коррозия, зависит от температурного режима. При высокой температуре окислительные процессы развиваются стремительнее. Причем снижение роли термодинамического фактора протекания реакции не влияет на процесс.
Немалое значение имеет охлаждение и переменный нагрев. Из-за термических напряжений в оксидной пленке появляются трещины. Через прорехи окислительный элемент попадает на поверхность. В результате образуется новый слой оксидной пленки, а прежний — отслаивается.
Не последнюю роль играют и компоненты газовой среды. Этот фактор индивидуален для разных видов металлов и согласуется с температурными колебаниями. К примеру, медь быстро поддается коррозии, если она контактирует с кислородом, но отличается устойчивостью к этому процессу в среде оксида серы. Для никеля же напротив, серный оксид губителен, а устойчивость наблюдается в кислороде, диоксиде углерода и водной среде. А вот хром проявляет стойкость ко всем перечисленным средам.
Обратите внимание! Если уровень давления диссоциации окисла превышает давление окисляющего элемента, окислительный процесс останавливается и металл обретает термодинамическую устойчивость.
На скорость окислительной реакции влияют и компоненты сплава. Например, марганец, сера, никель и фосфор никак не способствуют окислению железа. А вот алюминий, кремний и хром делают процесс более медленным. Еще сильнее замедляют окисление железа кобальт, медь, бериллий и титан. Сделать процесс более интенсивным помогут добавки ванадия, вольфрама и молибдена, что объясняется легкоплавкостью и летучестью данных металлов. Наиболее медленно окислительные реакции протекают при аустенитной структуре, поскольку она наиболее приспособлена к высоким температурам.
Еще один фактор, от которого зависит скорость коррозии, — характеристика обработанной поверхности. Гладкая поверхность окисляется медленнее, а неровная — быстрее.
Предотвращение ржавления
Отслаивающаяся краска обнажает участки ржавой поверхности листового металла.
Ржавчина является проницаемой для воздуха и воды, поэтому внутрилежащее железо продолжает разъедаться. Предотвращение ржавчины, следовательно, требует покрытия, которое исключает образование ржавчины. На поверхности нержавеющей стали образуется пассивирующий слой оксида хрома (III). Подобное проявление пассивации происходит с магнием, титаном, цинком, оксидом цинка, алюминием, полианилином и другими электропроводящими полимерами.
Гальванизация
Хорошим подходом к предотвращению ржавчины является метод гальванизации, который обычно заключается в нанесении на защищаемый объект слоя цинка либо методом горячего цинкования, либо методом гальванотехники. Цинк традиционно используется, потому что он достаточно дёшев, обладает хорошей адгезией к стали и обеспечивает катодную защиту на стальную поверхность в случае повреждения цинкового слоя. В более агрессивных средах (таких, как солёная вода), предпочтительнее кадмий. Гальванизация часто не попадает на швы, отверстия и стыки, через которые наносилось покрытие. В этих случаях покрытие обеспечивает катодную защиту металла, где оно выступает в роли гальванического анода, на который прежде всего и воздействует коррозия. В более современные покрытия добавляют алюминий, новый материал называется цинк-алюм
. Алюминий в покрытии мигрирует, покрывая царапины и, таким образом, обеспечивая более длительную защиту. Этот метод основан на применении оксидов алюминия и цинка, защищающих царапины на поверхности, в отличие от процесса оксидизации, как в случае применения гальванического анода. В некоторых случаях при очень агрессивных средах или длительных сроках эксплуатации применяются одновременно и гальванизация цинком, и другие защитные покрытия, чтобы обеспечить надёжную защиту от коррозии.
Катодная защита
Катодная защита является методом, используемым для предотвращения коррозии в скрытых под землёй или под водой структурах путём подачи электрического заряда, который подавляет электрохимические реакции. Если её правильно применять, коррозия может быть остановлена полностью. В своей простейшей форме это достигается путём соединения защищаемого объекта с протекторным анодом, в результате чего на поверхности железа или стали происходит только катодный процесс. Протекторный анод должен быть сделан из металла с более отрицательным электродным потенциалом, чем железо или сталь, обычно это цинк, алюминий или магний.
Лакокрасочные и другие защитные покрытия
От ржавчины можно предохранять с помощью лакокрасочных и других защитных покрытий, которые изолируют железо из окружающей среды. Большие поверхности, поделённые на секции, как например, корпуса судов и современных автомобилей, часто покрывают продуктами на основе воска. Такие средства обработки содержат также ингибиторы коррозии. Покрытие стальной арматуры бетоном (железобетон) обеспечивает некоторую защиту стали в среде с высоким pH. Однако коррозия стали в бетоне всё ещё является проблемой.
Покрытие слоем металла
Ржавчина может полностью разрушить железо. Обратите внимание на гальванизацию незаржавевших участков.
- Оцинковка (оцинкованное железо/сталь): железо или сталь покрываются слоем цинка. Может использоваться метод горячего цинкования или метод цинкового дутья.
- Лужение: мягкая листовая сталь покрывается слоем олова. В настоящее время практически не используется из-за высокой стоимости олова.
- Хромирование: тонкий слой хрома наносится электролитическим способом на сталь, обеспечивая как защиту от коррозии, так и яркий, полированный внешний вид. Часто используется в блестящих компонентах велосипедов, мотоциклов и автомобилей.
Воронение
Воронение — это способ, который может обеспечить ограниченную устойчивость к коррозии для мелких предметов из стали, таких как огнестрельное оружие и др. Способ состоит в получении на поверхности углеродистой или низколегированной стали или чугуна слоя окислов железа толщиной 1-10 мкм. Для придания блеска, а также для улучшения защитных свойств окисной плёнки, её пропитывают минеральным или растительным маслом.
Снижение влажности
Ржавчины можно избежать, снижая влажность окружающего железо воздуха. Этого можно добиться, например, с помощью силикагеля.
Ингибиторы
Ингибиторы коррозии, как, например, газообразные или летучие ингибиторы, можно использовать для предотвращения коррозии в закрытых системах. Некоторые ингибиторы коррозии чрезвычайно ядовиты. Одним из лучших ингибиторов выступают соли технециевой кислоты.
Средства для удаления ржавчины
Сегодня не редко встречается специальная краска по ржавчине. Она представлена на отечественном рынке большим количеством марок. Ее достоинством является то, что, она дает достаточно плотное покрытие. Она обладает тройным действием.
Она сочетает в себе функции:
- преобразователя ржавчины,
- грунтовки,
- красящего вещества с высоким уровнем плотности.
Она не только устраняет следы ржавчины, но и делает покрытие более ровным и привлекательным. Краски для работы с ржавыми предметами обладают высоким уровнем насыщенности цвета, чтобы даже в один слой скрывались все следы наличия ржавого налета. При этом на металле образуется небольшой слой пленки, который не дает ржавчине и дальне распространяться и развиваться новой.
Экономический эффект
Ржавчина вызывает деградацию изделий и конструкций, изготовленных из материалов на основе железа. Поскольку ржавчина имеет гораздо больший объём, чем исходное железо, её нарост ведёт к быстрому разрушению конструкции, усиливая коррозию на прилегающих к нему участках — явление, называемое поеданием ржавчиной
. Это явление стало причиной разрушения моста через реку Мианус (штат Коннектикут, США) в 1983 году, когда подшипники подъёмного механизма полностью проржавели изнутри. В результате этот механизм зацепил за угол одной из дорожных плит и сдвинул её с опор. Ржавчина была также главной причиной разрушения Серебряного моста в Западной Вирджинии в 1967 году, когда стальной висячий мост рухнул меньше, чем за минуту. Погибли 46 водителей и пассажиров, находившихся в то время на мосту.
Мост Кинзу после разрушения.
Мост Кинзу в штате Пенсильвания был снесён смерчем в 2003 году в значительной степени потому, что центральные опорные болты, соединяющие сооружение с землёй, проржавели, из-за чего мост держался лишь под действием силы тяжести.
Кроме того, коррозия покрытых бетоном стали и железа может вызвать раскалывание бетона, что создает серьёзные конструкторские трудности. Это один из наиболее распространённых отказов железобетонных мостов.