Графит
— минерал из класса самородных элементов, одна из аллотропных модификаций углерода. Распространенный в природе минерал. Встречается обычно в виде отдельных чешуек, пластинок и скоплений, разных по величине и содержанию графита. Различают месторождения кристаллического графита, связанного с магматическими горными породами или кристаллическими сланцами, и скрытокристаллического графита, образовавшегося при метаморфизме углей.
- Структура
- Свойства
- Морфология
- Происхождение
- Применение
- Классификация
- Физические свойства
- Оптические свойства
- Кристаллографические свойства
Смотрите так же:
Агат
– цена и лечебные, магические свойства
Физические свойства и структура алмаза
Графит в природе
В природе содержится в гранитах, пирите. Он образуется в магматических и вулканических горных породах, скарнах и пегматитах при высоких температурах, встречается в кварцевых жилах с различными материалами, широко распространен в мраморе, кристаллических сланцах, гнейсах. В результате пиролиза под воздействием на каменноугольные отложения траппов образуются крупные залежи природного минерала.
Показатели:
- Содержание минералов 2.0%
- Содержание углерода > 98.0%
- Содержание серы 550 ppm
- Температурный диапазон -200…3000°C
- Выщелачиваемый хлорид 50 ppm
- Сжимаемость 40%
- Регенерация 15%
- pH диапазон 0-14
- Проседание под нагрузкой <5%
ФИЗИЧЕСКИЕ СВОЙСТВА
| Цвет минерала | железно-чёрный переходящий в стально-серый |
| Цвет черты | чёрный переходящий в стально-серый |
| Прозрачность | непрозрачный |
| Блеск | полуметаллический |
| Спайность | весьма совершенная по {0001} |
| Твердость (шкала Мооса) | 1-2 |
| Излом | слюдоподобный |
| Прочность | гибкий |
| Плотность (измеренная) | 2.09 – 2.23 г/см3 |
| Радиоактивность (GRapi) | 0 |
Виды природного графита:
- тигельный (используется для производства огнеупорных изделий. Он отличается повышенной теплопроводностью и стойкостью к резким температурным перепадам),
- литейный кристаллический (имеет низкий коэффициент расширения, характеризуется прочностью при высоких температурах, используется при отливе деталей),
- аккумуляторный (применяется как добавка, графит используется для производства электродов, отличается повышенными техническими и химическими свойствами),
- для производства стержней для карандашей (тонкодисперсный, мягкий, не содержит примесей железа),
- элементный (графит используется для производства гальванических элементов, отличается повышенной тепло- и электропроводностью),
- электроугольный,
- для изготовления смазок и электропроводящей резины.
Свойства графита
Грифель карандаша изготавливается из графита, представляющего собой форму натурального углерода. Графит под влиянием давления и подогрева в почве обретает кристаллическую структуру. Его кристаллы напоминают пластины, объединённые непрочной связью.
Наиболее распространённый вид графита — аморфный, или сланцевый, кристалл, Известно, что такой грифель отличается рассыпчатостью и не подходит для рисования.
Около 1500 лет назад в Англии был обнаружен графит высокой плотности, где впоследствии его добывали на протяжении трёх лет. Графит, соответствующий описанию, применялся в изготовлении форм для пушечных ядер.
Качественный графит содержит высокий процент углерода. Кроме того, выяснилось, что грифель такого свойства имеет в своём составе наибольшую долю глины. Благодаря глине смесь сохраняет свою прочную консистенцию до момента обжига, а после него оказывает цементирующее воздействие.
Кристаллографические свойства
| Точечная группа | 6mm — дигексагонально-пирамидальный |
| Пространственная группа | P63mc |
| Сингония | гексагональная |
| Параметры ячейки | a = 2.461Å, c = 6.708Å |
| Двойникование | по {1121} |
Химические свойства графита
Графит взаимодействует с окислителями и с сильными восстановителями:
Понятие об аллотропии
Формула графита показывает, что в состав этого вещества входит только углерод в свободном виде. Хотя в природе он часто встречается и в виде соединений. Такими примерами являются углекислый и угарный газ, известняк, мел, мрамор.
Дело в том, что формула графита в химии такая же, как и у алмаза. Возможно ли это? Получается, что вещества с одинаковым составом имеют абсолютно разные свойства. Такое явление называется аллотропией. Она может быть обусловлена количеством атомов в молекуле вещества или их пространственным расположением. Примером первого случая является кислород. Если в молекуле два атома этого химического элемента, образуется кислород, а если три — озон.
Графит: формула, химическая и физическая характеристика
Как мы уже сказали, графит — это углерод. Соответственно, в химии записывается он как С. Несмотря на то что формула алмаза и графита сходна по качественному составу, эти вещества имеют значительные отличия в свойствах. Это объясняется разным пространственным расположением атомов углерода в их молекулах.
Графит — это мягкое вещество серого цвета с металлическим блеском. Оно без усилий расслаивается на мелкие пластинки и проводит электрический ток. Ученые доказали, что если графит нагреть до 1 600 градусов по шкале Цельсия под давлением 104 МПа при наличии катализаторов, то он превратится в алмаз. Таким способом в промышленности получают искусственные драгоценности.
Графит не является химически активным веществом. Он реагирует только с некоторыми солями и щелочными металлами. Продуктами таких реакций являются подобия включений. Сгорание графита в кислороде происходит только при очень высокой температуре с образованием углекислого газа. Однако он вступает в реакцию фторирования. При этом образуется порошок белого цвета, структура которого изменяется на зигзагообразную, приобретая лучшие смазочные свойства по сравнению с обычным графитом.
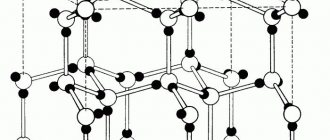
Структура
Рассматривая, какая плотность у графита, а также свойства и виды, необходимо уделить внимание его структуре. Это слоистое вещество. Его атомы углерода выстраиваются в кристаллическую решетку, похожую на соты. Шестиугольники в одном слое плотно прилегают друг к другу. Однако связь между каждым уровнем слаба. Именно эта особенность позволяет легко сломать графит.
По шкале Мооса твердость материала равна единице. Для сравнения, у алмаза этот показатель равен 10, а у керамогранита – 5. При температуре 1500°С, согласно исследованиям ученых, кристаллическая решетка графита может преобразовываться в алмаз.
В процессе промышленной обработки структура вещества меняется. Вместе с этим у разных марок графита определяются неодинаковые свойства. Если же добытый материал не был обработан искусственно, это природный тип вещества.
Оптические свойства
| Тип | одноосный (-) |
| Показатели преломления | nω = 1.93-2.07 |
| Анизотропия | чрезмерная |
| Цвет в отраженном свете | железно-чёрный переходящий в стально-серый |
| Плеохроизм | сильный, цвет красный |
| Люминесценция в ультрафиолетовом излучении | не флюоресцентный |
СВОЙСТВА
Хорошо проводит электрический ток. В отличие от алмаза обладает низкой твёрдостью (1 по шкале Мооса). Относительно мягкий. После воздействия высоких температур становится немного твёрже, и становится очень хрупким. Плотность 2,08—2,23 г/см³. Цвет тёмно-серый, блеск металлический. Неплавкий, устойчив при нагревании в отсутствие воздуха. Жирный (скользкий) на ощупь. Природный графит содержит 10—12 % примесей глин и окислов железа. При трении расслаивается на отдельные чешуйки (это свойство используется в карандашах).
Теплопроводность графита от 278,4 до 2435 Вт/(м*К), зависит от марки графита, от направления относительно базисных плоскостей и от температуры.
Электрическая проводимость монокристаллов графита анизотропна, в направлении, параллельном базисной плоскости, близка к металлической, в перпендикулярном — в сотни раз меньше. Минимальное значение проводимости наблюдается в интервале 300—1300 К, причём положение минимума смещается в область низких температур для совершенных кристаллических структур. Наивысшую электрическую проводимость имеет рекристаллизованный графит.
Коэффициент теплового расширения графита до 700 К отрицателен в направлении базисных плоскостей (графит сжимается при нагревании), его абсолютное значение с повышением температуры уменьшается. Выше 700 К коэффициент теплового расширения становится положительным. В направлении, перпендикулярном базисным плоскостям, коэффициент теплового расширения положителен, практически не зависит от температуры и более чем в 20 раз выше среднего абсолютного значения для базисных плоскостей.
Монокристаллы графита диамагнитны, магнитная восприимчивость незначительна в базисной плоскости и велика в ортогональных базисным плоскостях. Коэффициента Холла меняется с положительного на отрицательный при 2400 К.
Морфология
Хорошо образованные кристаллы редки. Кристаллы пластинчатые, чешуйчатые, кривогранные, обычно имеют пластинчатую несовершенную форму. Чаще бывает представлен листочками без кристаллографических очертаний и их агрегатами. Образует сплошные скрытокристаллические, листоватые или округлые радиально-лучистые агрегаты, реже — сферолитовые агрегаты концентрически-зонального строения. У крупнокристаллических выделений часто наблюдается треугольная штриховка на плоскостях (0001).
Кристаллографические свойства
| Точечная группа | 6 mm — дигексагонально-пирамидальный |
| Пространственная группа | P63mc |
| Сингония | гексагональная |
| Параметры ячейки | a = 2.461Å, c = 6.708Å |
| Двойникование | по {1121} |
Месторождения
Самые большие залежи графита расположены в Китае, Украине, Мексике, Канаде и Южной Корее. Месторождения минерала экономически выгодны для страны, на территории которой он расположен. В процессе разработки залежей обеспечение промышленности нужным сырьём. Камнем образованы скопления серого цвета. Графитовая руда добывается открытым способом, а кусковой минерал подземным методом.
Одним из высокотемпературных жильных залежей минералов стоит выделить месторождение на Цейлоне, которое обладает большим промышленным значением. Здесь графитовые жилы расположены среди гнейсов. Такие же месторождения есть в Квебеке, штате Монтана и Англии.
Где и как добывается
Залежи графита промышленных объемов есть на всех континентах:
- Обе Америки – США, Канада, Бразилия;
- Европа – ФРГ, Гренландия, Италия;
- Австралия.
Сырье каждого графитового рудника можно отличить по структуре, цвету, другим признакам.
Россия располагает тремя крупнейшими месторождениями:
- Бурятия – качественное плотнокристаллическое сырье.
- Краснодарский край (два) – плотно-, мелкокристаллический, чешуйчатый, графитовые сланцы.
Графиты формируются каменноугольным пиролизом либо под влиянием экстремально высоких температур и давления. Например, излияниями магмы на отложения каменного угля.
Его добывают наземным или подземным способами. Графитовые кристаллы находят в сланцах, мраморах, других органических породах.
Ежегодный мировой объем добычи графита – 600 тыс. тонн.
Запасы
Мировые запасы графита (1978, тысяч т) в капиталистических и развивающихся странах: чешуйчатого — Южная Америка, 136; Европа, 3500; Африка, 5442; Азия, 900; плотнокристаллического — Азия, 2900; скрытокристаллического — Северная Америка (без США), 3084; Европа, 5623; Азия, 6168. О добыче графита см. в ст. графитовая промышленность.
Разновидности
Природный графит многообразен, поэтому разработана классификация по нескольким признакам.
По составу и сферам применения:
- Коллоидный. Техническая разновидность, порошок из искусственного графита. Используется промышленностью.
- Пиролитический. Материал искусственного происхождения. Нашел применение как основа инструментария для исследований микроструктур.
- Силицированный. Графит, обогащенный кремнием. Устойчив к коррозии.
Природный графит по структуре подразделяют на волокнистый, плотнокристаллический, чешуйчатый, графитовый сланец. Выделяют также разновидности – графитит и графитовую слюдку.
Сферы применения
Свойства графита позволяют его применять и в повседневной жизни, и в промышленности. Благодаря высокой огнеупорности и электропроводимости его применяют в металлургии для производства форм и ковшей. Литейные предприятия используют порошок в качестве смазки.
Кроме того, графит добавляется в состав огнеупорного кирпича, шлифовальных и полировочных растворов. Самое известное применение — изготовление карандашей для рисования. Даже сфера атомной энергетики применяет его на своих объектах.
Одной из самых качественных красок считается именно графитовая. С помощью такой смеси можно обеспечить эффективную защиту чугунных, алюминиевых, деревянных и бетонных изделий от воздействия коррозии.
В медицинской сфере графит применяется при лечении болезней кожи, которые представляют собой следствие самых разных внутренних нарушений. Также этот элемент предотвращает формирование рубцов и спаек после серьезных воспалений и оказывает положительное влияние на процессы обмена веществ. Именно поэтому его добавляют во многие лекарства.
Как производят графитовые стержни
Самая ответственная операция в производстве стержней — помол графита. Чем мельче будут частицы, тем более гладкими получатся стержни, тем лучше они будут писать. Механические способы помола требуют длительного времени, и все равно достаточно мелких частиц не получается. Поэтому применяют механохимические методы, в вибрационную или струйную мельницу вводят поверхностно- активное вещество, которое смачивает измельченные частицы и не дает им вновь слипаться. В результате размеры частиц графита получаются ничтожными — около одного микрона.
Для наглядности хотелось бы сравнить их с чем-нибудь известным, но даже самая тонкая пудра грубее, чем карандашный графит. А вот глину измельчать не надо, она и так достаточно мелка: у ее частиц субмикроскопические размеры. Графит смешивают с глиной. От того, в каком соотношении смешивают, и зависит твердость будущего стержня. Самый твердый получится из чистой глины, самый мягкий — из чистого графита Конечно, обе эти крайности абсурдны. Просто в 6Т очень мало графита, в 6М его очень много.
Смесь графита с глиной продавливают через сопло и непрерывную черную змейку автоматически режут на отдельные стержни. А потом отправляют в печь. Глины для карандашей состоят из каолинита. При высоких температурах из него выделяется вода и образуется плотный полимер. Поэтому стержень становится прочным, водостойким и более упругим, твердость его возрастает на одну — полторы градации.
Но из-за испарения воды стержень после обжига буквально насыщен мельчайшими сообщающимися между собой порами, проведенная им линия прерывиста и неравномерна. Приходится пропитывать обожженный стержень восками — годным, японским, карнаубским — или воскоподобными веществами вроде стеарина. Кстати, такие вещества заодно улучшают сцепление написанного с бумагой и уменьшают трение при письме.
Искусственный графит — область применения
Искусственно производится конструкционный, мелкозернистый, антифрикционный и литейный графит. Область применения материала достаточно широкая. Графит используется для изготовления огнеупорных материалов, электрических машин и установок, в химической, горнодобывающей промышленности, а также на производстве. Из него также изготавливают стержневые карандаши, краски, покрытия и аккумуляторные батареи. Графит незаменим в ядерной промышленности и в других узконаправленных областях.
Применение в пищевой промышленности
Представленное вещество также широко применяется в пищевой промышленности. Для этого при производстве оно подвергается определенной обработке. Плотность железа, этилового спирта, графита и сахара, по понятным причинам, различна. Но представленный материал может как содержать в себе, так и входить в состав некоторых веществ. Он находится в парафинах, эфирах, спирте и даже в сахаре.
В этом можно убедиться, если провести несложный опыт. Сначала нужно взять кусочек сахара. Его кладут на твердую крышку и накрывают колпачком (можно наперстком). Затем металл, которым накрыт сахар, сильно нагревают. Из-под наперстка со временем станет выделяться едкий дым. Если к нему поднести спичку, газ станет гореть.
Когда дым перестанет выделяться, можно снять наперсток. На крышке остается черная масса. Это уголь. Он представляет собой углерод, из которого и состоит графит.
Где используется
Графит почти универсален. В этом нет ничего необычного: необходимые характеристики закладываются на стадии его обработки. Так, одним требуется повышенная теплопроводность, другим – электропроводность. Третьих интересуют прочностные свойства графита.
С учетом кондиций готового продукта минерал востребован для следующих целей:
- Производство тугоплавких емкостей.
- Смазка при выплавке стали, сплавов.
- Стержни ядерных реакторов на АЭС, других агрегатах.
Сувенирный графитовый блок - Добавка к составу пластиковых изделий, огнеупоров (керамики, кирпича).
- Исходник частей электроприборов, подшипников, автомобильных рессор.
- Краска, используемая промышленностью и в быту как защитное покрытие от ржавчины.
- Сырье при изготовлении искусственных алмазов.
- Ингредиент лекарств, пищевых парафинов, эфирных субстанций, спиртов, сахара.
Самое известное применение графита – сердцевина карандашей.
Московские ученые создали из графита лекарство для лечения кожных заболеваний.
Стоимость материала
Реализацией графита и его смесей занимаются специальные организации, добывающие и получающие материал. Стоимость его находится на вполне приемлемом уровне и зависит от содержания углерода и габаритов кристалликов. У каждого сорта есть своя цена — чем больше в материале углерода, тем, соответственно, он дороже и имеет лучшие технические характеристики.
Продается графит как оптом, так и в розницу. Примечательно, что при оптовой покупке можно получить очень неплохую скидку.
Стоимость материала также зависит и от региона продажи. Средняя же цена составляет примерно 45−50 рублей за 1 кг. Графитовые изделия имеют большую стоимость.
Ионный тип
Противоположно заряженные ионы находятся на узлах, которые создают электромагнитное поле, характеризующее физические свойства вещества. К таковым будут относиться: электропроводность, тугоплавкость, плотность и твёрдость. Поваренная соль и нитрат калия характеризуются наличием ионной кристаллической решётки.
Не пропустите: механизм образования металлической связи, конкретные примеры.
Различия между алмазом и графитом
Несмотря на то что минералы имеют схожие химические формулы, они резко отличаются друг от друга как внешним видом, так и с химической точки зрения.
Прежде всего, алмаз и графит имеют совершенно различную друг от друга структуру. Ведь графит состоит из сетки шестиугольников, тогда как алмаз имеет кубическую кристаллическую структуру. Хрупкость графита обуславливается тем, что связь между его слоями нарушить очень легко, его атомы спокойно отделяются друг от друга. Из-за этого графит легко поглощает свет, сам он очень темный, в отличие от алмаза.
Структура алмаза отличается тем, что один атом углерода окружен еще четырьмя атомами в виде четырехгранного треугольника или пирамиды. Каждый атом находится на одинаковом расстоянии друг от друга. Связь у атомов очень крепкая, именно поэтому алмаз является таким твердым и прочным. Еще одно свойство алмаза — это то, что он может проводить свет, в отличие от графита.
Странно ли, что формула графита совпадает с формулой алмаза, но при этом минералы совершенно разные? Нет! Ведь алмаз создается природой при огромном давлении, а затем очень быстром охлаждении, тогда как графит возникает при низком давлении, но очень высокой температуре.
СТРУКТУРА
Гексагональная кристаллическая полиморфная (аллотропная) модификация чистого углерода, наиболее устойчивая в условиях земной коры. Слои кристаллической решетки могут по-разному располагаться относительно друг друга, образуя целый ряд политипов, с симметрией от гексагональной сингонии (дигексагонально-дипирамидальный вид симметрии), до тригональной (дитригонально-скаленоэдрический в.с.). Кристаллическая решетка графита – слоистого типа. В слоях атомы С расположены в узлах гексагональных ячеек слоя. Каждый атом С окружен тремя соседними с расстоянием 1,42Α
Различают две модификации графита: α-графит (гексагональный P63/mmc) и β-графит (ромбоэдрический R(-3)m). Различаются упаковкой слоёв. У α-графита половина атомов каждого слоя располагается над и под центрами шестиугольника (укладка …АВАВАВА…), а у β-графита каждый четвёртый слой повторяет первый. Ромбоэдрический графит удобно представлять в гексагональных осях, чтобы показать его слоистую структуру.
β-графит в чистом виде не наблюдается, так как является метастабильной фазой. Однако, в природных графитах содержание ромбоэдрической фазы может достигать 30 %. При температуре 2500-3300 К ромбоэдрический графит полностью переходит в гексагональный.
Получение алмаза из графита
Формула графита — C — позволила ученым произвести множество опытов, вследствие чего были найдены аллотропные вещества графита.
Преподаватели рассказывают и школьникам, и студентам о том, как ученые пытались создать алмазы из графита. Эта история очень интересная и увлекательная, а еще она позволяет запомнить о существовании таких аллотропных веществ, как графит и алмаз, и об их различиях.
Некоторое время назад ученые пытались создать алмазы из графита. Они считали, что если формула алмаза и графита одинакова, то они смогут создать алмаз, ведь камень очень дорогой и редкий. Теперь мы знаем, что минерал алмаз появляется в природе при высоком давлении и мгновенном охлаждении. Поэтому ученые решили взорвать ѓрафит, тем самым создав нужные условия для образования алмаза. И на самом деле случилось чудо, после взрыва на графите образовались очень маленькие кристаллы алмаза.
История
История и время формирования графита остается загадкой для науки: он слишком похож на другие минералы по описанию.
Единственная зацепка – глиняная утварь культуры Боян-Марицы (территория современных Болгарии и Румынии, 6 тыс. лет назад). Изделия раскрашены графитовыми красками.
Графитом минерал предложил именовать Абраам Вернер. Этот прославленный химик, «окрестивший» десятки камней, взял за основу свойство минерала оставлять четкий красящий след.
Древнегреческий термин γράφω означает «пишу».
На территории России графит найден в 1826 году на Урале.
В истории, литературе минерал фигурирует также как черный/серебристый свинец, карбидное железо.
Лечебное влияние
Первыми оценили графит гомеопаты. Они установили, что минерал подходит для лечения кожных патологий (экземы, псориаз, лишай, другие).
Сегодня список расширен:
- Нарушение обмена веществ.
- Сбой в работе щитовидной железы.
- Заболевания дыхательных путей (ринит, бронхиальная астма).
- Проблемы ЖКТ (гастрит, язва желудка, 12-перстной кишки, колиты).
- Женские недуги (аменорея, хроническое воспаление яичников, мастопатия).
- Конъюнктивит, катаракта, ячмень.
Минерал «курирует» также эмоциональное здоровье. Его прописывают при утренней головной боли, неврастении, апатии, депрессии.
Источники
- https://vseprokamni.ru/vidy/organicheskie/ximicheskaya-formula-grafita.html
- https://FB.ru/article/351885/chto-takoe-grifel-i-v-ch-m-zaklyuchayutsya-ego-unikalnyie-svoystva-dlya-risovaniya
- https://mineralpro.ru/minerals/graphite/
- https://www.syl.ru/article/307195/formula-grafita-allotropiya-ugleroda
- https://FB.ru/article/277065/grafit-plotnost-svoystva-osobennosti-primeneniya-i-vidyi
- https://vseprokamni.ru/svoistva/kristallicheskaja-reshetka-grafita.html
- https://crystal-wow.ru/kamni/fizicheskie-svojstva-grafita-tablica.html
- https://vseprokamni.ru/svoistva/fizicheskie-i-himicheskie-svojstva-granita.html
- https://natrukodel.ru/prochie/himicheskaya-formula-grafita
- https://abc-24.info/prostoj-karandash-istoriya/
- https://FB.ru/article/236131/allotropnyie-veschestva-almaz-i-grafit-formula-grafita-i-almaza