ХРОМ
– (Chromium) Cr, химический элемент 6(VIb) группы Периодической системы. Атомный номер 24, атомная масса 51,996. Известно 24 изотопа хрома с 42Cr по 66Cr. Изотопы 52Cr, 53Cr, 54Cr являются стабильными. Изотопный состав природного хрома: 50Cr (период полураспада 1,8·1017 лет) – 4,345%, 52Cr – 83,489%, 53Cr – 9,501%, 54Cr – 2,365%. Основные степени окисления +3 и +6.
Также по теме:
ХИМИЯ
В 1761 профессор химии Петербургского университета Иоганн Готтлоб Леман (Johann Gottlob Lehmann) у восточного подножия Уральских гор на Березовском руднике обнаружил замечательный красный минерал, который при измельчении в порошок давал яркую желтую окраску. В 1766 Леман привез образцы минерала в Петербург. Обработав кристаллы соляной кислотой, он получил белый осадок, в котором обнаружил свинец. Леман назвал минерал сибирским красным свинцом (plomb rouge de Sibérie), теперь известно, что это был крокоит (от греческого «krokos» – шафран) – природный хромат свинца PbCrO4.
Немецкий путешественник и естествоиспытатель Петер Симон Паллас (Peter Simon Pallas) (1741–1811) возглавил экспедицию Петербургской Академии наук в центральные регионы России и в 1770 побывал на Южном и Среднем Урале, в том числе на Березовском руднике и, подобно Леману, заинтересовался крокоитом. Паллас писал: «Этот удивительный красный свинцовый минерал не встречается более ни в одном месторождении. При растирании в порошок становится желтым, и может быть использован в художественной миниатюре». Несмотря на редкость и трудность доставки крокоита с Березовского рудника в Европу (на это уходило почти два года), использование минерала в качестве красящего вещества было оценено по достоинству. В Лондоне и Париже конца 17 в. все знатные особы ездили на каретах, покрашенных мелко растертым крокоитом, кроме того, лучшие образцы сибирского красного свинца пополняли коллекции многих минералогических кабинетов Европы.
Также по теме:
ХРОМАТЫ И ДИХРОМАТЫ
В 1796 образец крокоита попал к профессору химии Парижской минералогической школы Никола Луи Вокелену (Nicolas-Louis Vauquelin) (1763–1829), который проанализировал минерал, но не нашел в нем ничего кроме оксидов свинца, железа и алюминия. Продолжая исследования сибирского красного свинца, Вокелен прокипятил минерал с раствором поташа и после отделения белого осадка карбоната свинца получил желтый раствор неизвестной соли. При обработке его солью свинца образовывался желтый осадок, солью ртути – красный, а при добавлении хлорида олова раствор становился зеленым. Разлагая крокоит минеральными кислотами, он получил раствор «кислоты красного свинца», упаривание которой давало рубиново-красные кристаллы (сейчас понятно, что это был хромовый ангидрид). Прокалив их с углем в графитовом тигле, обнаружил после реакции множество сросшихся серых игольчатых кристаллов неизвестного до того времени металла. Вокелен констатировал высокую тугоплавкость металла и его устойчивость по отношению к кислотам.
Вокелен назвал новый элемент хромом (от греческого crwma – цвет, окраска) ввиду множества образуемых им разноцветных соединений. На основании своих исследований Вокелен впервые констатировал, что изумрудная окраска некоторых драгоценных камней объясняется примесью в них соединений хрома. Например, природный смарагд представляет собой окрашенный в глубокий зеленый цвет берилл, в котором алюминий частично замещен хромом.
Скорее всего, Вокеленом был получен не чистый металл, а его карбиды, о чем свидетельствует игольчатая форма полученных кристаллов, но Парижская Академия наук тем не менее зарегистрировала открытие нового элемента, и сейчас Вокелен справедливо считается первооткрывателем элемента № 24.
В 1798 Ловиц и Клапрот (Klaproth) независимо от Вокелена обнаружили хром в образце тяжелого черного минерала (это был хромит FeCr2O4), найденного на Урале, но значительно севернее Березовского месторождения. В 1799 Ф.Тассерт (Tassaert) обнаружил новый элемент в том же минерале, найденном на юго-востоке Франции. Считается, что именно Тассерту впервые удалось получить относительно чистый металлический хром.
Что представляет собой
Хром – это металл, элемент таблицы Менделеева №24.
Международное обозначение и формула – Chromium, Cr.
Серебристо-голубоватое блестящее вещество – одно из самых твердых (5,5 по Моосу) и тугоплавких металлов, но хрупко. Относится к чёрным металлам.
Структура, свойства роднят его с железом, марганцем, титаном, никелем. Эти элементы объединены в одно семейство.
Уникальная особенность элемента – ярко-радужная окраска соединений: голубизна, фиолет, зелень до изумрудности, желтизна, оранж, пурпур. Они обусловили название, благодаря им легко отличить хром от других металлов.
По-древнегречески χρῶμα (хрома) – краска, цвет.
История открытия Хром Chromium
Открытие элемента Chromium на Среднем Урале, в Березовском золоторудном месторождении. Впервые упоминается в труде М. В. Ломоносова «Первые основания металлургии» (1763 год), как красная свинцовая руда, PbCrO4. Современное название — крокоит. В 1797 году французский химик Л. Н. Воклен выделил из него новый тугоплавкий металл (скорее всего, Воклен получил карбид хрома). Он прокалил зелёный оксид Cr2O3 с углем и выделил тугоплавкий металл (с примесью карбидов). Сам оксид Cr2O3 Воклен получил разложением «Сибирского красного свинца» — минерала крокоита PbCrO4.
Современный способ получения чистого хрома (с 1894 г.) отличается от способа Воклена только видом восстановителя. Процесс электролитического покрытия железа хромом разработан в 20-х годах ХХ в.
Физико-химические характеристики
Физические и химические свойства хрома типичны для металлов:
- Химически малоактивен. В обычных условиях не взаимодействует с водой, растворами щелочей. Реакция запускается при +600°С.
- Кислород создает на его поверхности защитную оксидную пленку.
- В соединениях проявляет три степени: +2, +3, +6. Самые устойчивые – трехвалентные.
Применение хрома затрудняют недостатки:
- Явное ухудшение характеристик примесями в составе.
- Необходимость дополнительной обработки сверхтвердого металла для получения пластичности.
Однако они компенсируются достоинствами металла: тугоплавкостью, твердостью (пятый среди металлов), стойкостью к коррозии.
| Свойства атома | |
| Название, символ, номер | Хром / Chromium (Cr), 24 |
| Атомная масса (молярная масса) | 51,9961(6) а. е. м. (г/моль) |
| Электронная конфигурация | [Ar] 3d5 4s1 |
| Радиус атома | 130 пм |
| Химические свойства | |
| Ковалентный радиус | 118 пм |
| Радиус иона | (+6e)52 (+3e)63 пм |
| Электроотрицательность | 1,66 (шкала Полинга) |
| Электродный потенциал | −0,74 |
| Степени окисления | 6, 3, 2, 0 |
| Энергия ионизации (первый электрон) | 652,4 (6,76) кДж/моль (эВ) |
| Термодинамические свойства простого вещества | |
| Плотность (при н. у.) | 7,19 г/см³ |
| Температура плавления | 2130 K (1856,9 °C) |
| Температура кипения | 2945 K (2671,9 °C) |
| Уд. теплота плавления | 21 кДж/моль |
| Уд. теплота испарения | 342 кДж/моль |
| Молярная теплоёмкость | 23,3 Дж/(K·моль) |
| Молярный объём | 7,23 см³/моль |
| Кристаллическая решётка простого вещества | |
| Структура решётки | кубическая объёмноцентрированая |
| Параметры решётки | 2,885 Å |
| Температура Дебая | 460 K |
| Прочие характеристики | |
| Теплопроводность | (300 K) 93,9 Вт/(м·К) |
| Номер CAS | 7440-47-3 |
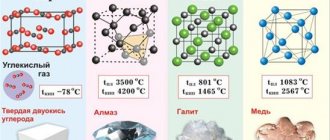
Кристаллическая решётка хрома:
| 500 | Кристаллическая решётка | |
| 511 | Кристаллическая решётка #1 | |
| 512 | Структура решётки | Кубическая объёмно-центрированная |
| 513 | Параметры решётки | 2,885 Å |
| 514 | Отношение c/a | |
| 515 | Температура Дебая | 460 K |
| 516 | Название пространственной группы симметрии | Im_ 3m |
| 517 | Номер пространственной группы симметрии | 229 |
Нахождение в природе
В природе отмечено два десятка хромовых минералов. Основные – хромит и крокоит.
Изверженные породы содержат разную концентрацию элемента (г/т):
- ультраосновные – 2000;
- базальты, другие основные – 200.
Каждая тонна земной коры содержит в среднем 83 г хрома.
Промышленный интерес представляет один класс – хромшпинелиды.
Металл содержат драгоценные камни – хромтурмалин, уваровит (хромовый гранат), другие.
Тяжелые металлы
Что такое тяжелые металлы
Особое значение приобрело загрязнение биосферы группой полютантов, получивших общее название «тяжелые металлы». К ним относится более 40 химических элементов периодической системы Д. И. Менделеева.
Тяжелыми металлами являются хром, марганец, железо, кобальт, никель, медь, цинк, галлий, германий, молибден, кадмий, олово, сурьма, теллур, вольфрам, ртуть, таллий, свинец, висмут. Употребляемый иногда термин «токсические элементы» здесь неудачен, так как любые элементы и их соединения могут стать токсичными для живых организмов при определенной концентрации и условиях окружающей среды.
Главным природным источником тяжелых металлов являются породы (магматические и осадочные) и породообразующие минералы. Многие минералы в виде высокодисперсных частиц включаются в качестве акцессорных (микропримесей) в массу горных пород. Примером таких минералов являются минералы титана (брусит, ильменит, анатаз), хрома (FeCr2O4). Многие элементы поступают в атмосферу с космической и метеоритной пылью, с вулканическими газами, горячими источниками, газовыми струями.
Поступление тяжелых металлов в биосферу вследствие техногенного рассеивания осуществляется разнообразными путями. Важнейшим из них является выброс при высокотемпературных процессах в черной и цветной металлургии, при обжиге цементного сырья, сжигании минерального топлива. Кроме того, источником загрязнения биоценозов могут служить орошение водами с повышенным содержанием тяжелых металлов, внесение осадков бытовых сточных вод в почвы в качестве удобрения. Вторичное загрязнение происходит также вследствие выноса тяжелых металлов из отвалов рудников или металлургических предприятий водными или воздушными потоками, поступления больших количеств тяжелых металлов при постоянном внесении высоких доз органических, минеральных удобрений и пестицидов, содержащих тяжелые металлы.
Часть техногенных выбросов тяжелых металлов, поступающих в атмосферу в виде аэрозолей, переносится на значительное расстояние и вызывает глобальное загрязнение. Другая часть с гидрохимическим стоком попадает в бессточные водоемы, где накапливается в водах и донных отложениях и может стать источником вторичного загрязнения. Соединения тяжелых металлов сравнительно быстро распространяются по объемам водного объекта. Частично они выпадают в осадок в виде карбонатов, сульфатов, частично адсорируются на минеральных и органических осадках. В результате содержание тяжелых металлов в отложениях постоянно растет, и когда абсорбционная способность осадков исчерпывается и тяжелые металлы поступают в воду, возникает особо напряженная ситуация. Этому способствует повышение кислотности воды, сильное зарастание водоемов, интенсификация выделения СО2 в результате деятельности микроорганизмов. Значительное загрязнение тяжелыми металлами, особенно свинцом, а также цинком и кадмием обнаружено вблизи автострад. Ширина придорожных аномалий свинца в почве достигает 100 м и более.
Тяжелые металлы, поступающие на поверхность почвы, накапливаются в почвенной толще, особенно в верхних гумусовых горизонтах, и медленно удаляются при выщелачивании, потреблении растениями, эрозии. Первый период полуудаления (т.е. удаления половины от начальной концентрации) тяжелых металлов значительно варьируется у различных элементов и занимает весьма продолжительный период времени: для цинка — от 70 до 510 лет; кадмия от 13 до 11О лет, меди -от 310 до 1500 лет, свинца — от 770 до 5900 лет.
Тяжелые металлы способны образовывать сложные комплексные соединения с органическими веществами почвы, поэтому в почвах с высоким содержанием гумуса они менее доступны для полощения. Избыток влаги в почве способствует переходу тяжелых металлов в низшие степени окисления и в растворимые формы. Анаэробные условия повышают доступность тяжелых металлов растениям. Поэтому дренажные системы, регулирующие водный режим, способствуют преобладанию окисленных форм тяжелых металлов и тем самым снижению их миграционных характеристик. Растения могут поглотать из почвы микроэлементы, в том числе тяжелые металлы, аккумулируя их в тканях или на поверхности листьев, являясь, таким образом, промежуточным звеном в цепи «почва — растение — животное — человек».
Различные растения сосредоточивают в себе разное число микроэлементов: в большинстве случаев — избирательно. Так, медь усваивают растения семейства гвоздичных, кобальт — перцы. Высокий коэффициент биологического поглощения цинка характерен для березы карликовой и лишайников, никеля и меди — для вероники и лишайников. Тяжелые металлы являются протоплазматическими ядами, токсичность которых возрастает по мере увеличения атомной массы. Их токсичность проявляется по-разному. Многие металлы при токсичных уровнях концентраций ингибируют деятельность ферментов (медь, ртуть). Некоторые из них образуют хелатоподобные комплексы с обычными метаболитами, нарушая нормальный обмен веществ (железо). Такие металлы, как кадмий, медь, железо, взаимодействуют с клеточными мембранами, изменяя их проницаемость.
Особый интерес представляет изучение животных, являющихся чувствительным индикатором начальных стадий загрязнения тяжелыми металлами. Они аккумулируют элементы в доступных биологически активных формах и отражают фактический уровень загрязнения экосистем. Почвенные животные, особенно сапрофитные группы, благодаря тесной связи с почвенными условиями и ограниченной территорией обитания могут быть хорошими индикаторами химического загрязнения биосферы. Среди животных такими индикаторами могут быть европейский крот, бурый медведь, лось, рыжая полевка. Располагая сведениями о содержании тяжелых металлов у млекопитающих, можно прогнозировать их влияние на организм человека.
Технология получения
Традиционное сырье для получения хрома – хромшпинелиды.
Главные способы получения металла – обогащение руды методом электролиза либо восстановлением.
Для повышения степени чистоты конечного продукта сырье сплавляют в электропечи с содой, добавляя кислород.
Производство металлического хрома почти абсолютной чистоты ведется методом электролиза концентрированных хромовых растворов либо восстановлением оксида хрома алюминием в вакуумных печах (при 1500°C).
Классификация и свойства
Элементы могут быть классифицированы на основе их физических состояний (состояний материи), например, газообразный, твёрдый или жидкий. Cr является твёрдым элементом. Он классифицируется в химии как «переходный металл», который находится в группах 3−12 Периодической таблицы Менделеева. Элементы, классифицируемые как переходные металлы, обычно описываются как пластичные и способные проводить электричество и тепло.
Химические свойства — это характеристики, которые становятся очевидными, когда материал подвергается химической реакции или химическим изменениям. Фактическая структура материала должна быть изменена, чтобы можно было наблюдать химические свойства.
- Взаимодействие с неметаллами. При нагревании выше 600 °C Cr сгорает в кислороде. С F реакция наступает при 350 °C, с Cl — при 300 °C, с Br — при t красного каления, образуя галогениды хрома (III).С N — при t выше 1000 °C с образованием нитридов.
- Взаимодействие с кислотами. В NCl и HCl в высокой концентрации Cr может растворяться только при сильном нагревании, образуя соли Cr (III) и продукты восстановления кислоты. При взаимодействии солей металла Cr и азотной кислоты образуется нитрат хрома Cr (NO3)3.
Это серо-голубой металл, который можно отполировать, чтобы добиться высокого блеска. Он очень блестящий, и хотя хром относительно твёрдый, он также и очень хрупкий. Это довольно активный металл. Хотя он не реагирует с водой, но он способен реагировать с большинством кислот, а также с кислородом при комнатной температуре. Одним из наиболее важных свойств Cr является его пассивация. Несмотря на то что он стабилен на воздухе, он тем не менее окисляется, образуя тонкий слой, который действует как защитное покрытие для предотвращения дальнейшей коррозии.
Cr в элементарной форме проявляет парамагнитные свойства. Недавно было обнаружено, что этот элемент может проявлять различные магнитные свойства в зависимости от его нагрева и охлаждения, а это, в свою очередь, влияет на ориентацию вращения электронов. Соединения элемента, такие как диоксид хрома, считаются ферромагнитными. Ферромагнитные свойства этих соединений позволяют использовать их в ленте данных, как способе хранения информации.
Cr можно добавлять к другим соединениям, сохраняя его магнитные свойства. Это зависит от количества других элементов в соединении.
Например, некоторые соединения из нержавеющей стали являются магнитными в зависимости от количества хрома, который они содержат.
Где используется
Металл используется по двум направлениям: как лигатура к другим металлам и как покрытие.
Металлургия
Отрасль, забирающая три четверти объемов металла. Хромом легируют стали для улучшения кондиций.
Получают продукт:
- нержавеющий;
- износостойкий;
- жаропрочный.
Такие достоинства сталей обусловили их применение как материала стволов артиллерии, корпусов субмарин, сейфов, металлорежущего, медицинского, химического инструментария. Из них выполнены двигатели космических кораблей, начинка плазмотронов.
Даже незначительное количество хрома в составе кратно улучшает механические свойства материала.
Самые известные хромсодержащие сплавы – с никелем (нихром) и железом (фехраль). Это прецизионные материалы с повышенным электрическим сопротивлением. Используются для работы при экстремальных температурах.
Другие отрасли промышленности
Продукция из металла и сплавов с ним выпускается для разных сегментов рынка:
- Кирпичи – корпус металлургических печей.
- Нагревательные элементы (сплав с никелем).
- Хирургический инструментарий (сплав с никелем, молибденом, кобальтом).
- Соединения хрома пригождаются при производстве спичек, обуви, одежды (знаменитая блестяще-прочная хромовая кожа), окраске текстиля, обработке мебельной древесины.
- Зеленую хромовую краску наносят на керамику перед покрытием глазурью и обжигом.
Краски из перетертых хромовых руд применяли еще иконописцы Древней Руси.
- Трехвалентный оксид металла – исходник при выращивании синтетических рубинов для лазеров.
- Зеленые огни салюта – заслуга хрома.
Хром закупают фармацевтические гиганты, производители биодобавок, препаратов для похудения.
Декор
Хромированное покрытие корпуса часов либо деталей авто – не только маркер статусности. Такая обработка защищает от износа, коррозии, механических повреждений.
Толщина покрытия металлом зависит от назначения изделия: от 2 мкм (декоративный ассортимент) до 0,1 мм (детали байков, велосипедов, авто).
Процесс покрытия хромом называется хромированием. Он технологически прост и недорог.
Понятие термического сопротивления и коэффициента теплопроводности
Если теплопроводность характеризует способность металлов передавать температуру тел от одной поверхности к иной, то термическое сопротивление показывает обратную зависимость, т.е. возможность металлов препятствовать такой передаче, иначе выражаясь, – сопротивляться. Высоким термическим сопротивлением обладает воздух. Именно он, больше всего, препятствует передаче тепла между телами.
Количественную характеристику изменения температуры единицы площади за единицу времени на один градус (К), называют коэффициентом теплопроводности. Международной системой единиц принято измерять этот параметр в Вт/м*град. Эта характеристика очень важна при выборе металлических изделий, которые должны передавать тепло от одного тела к другому.
Таблица 1
| Металл | Коэффициент теплопроводности металлов при температура, °С | ||||
| — 100 | 0 | 100 | 300 | 700 | |
| Алюминий | 2,45 | 2,38 | 2,30 | 2,26 | 0,9 |
| Бериллий | 4,1 | 2,3 | 1,7 | 1,25 | 0,9 |
| Ванадий | — | — | 0,31 | 0,34 | — |
| Висмут | 0,11 | 0,08 | 0,07 | 0,11 | 0,15 |
| Вольфрам | 2,05 | 1,90 | 1,65 | 1,45 | 1,2 |
| Гафний | — | — | 0,22 | 0,21 | — |
| Железо | 0,94 | 0,76 | 0,69 | 0,55 | 0,34 |
| Золото | 3,3 | 3,1 | 3,1 | — | — |
| Индий | — | 0,25 | — | — | — |
| Иридий | 1,51 | 1,48 | 1,43 | — | — |
| Кадмий | 0,96 | 0,92 | 0,90 | 0,95 | 0,44 (400°) |
| Калий | — | 0,99 | — | 0,42 | 0,34 |
| Кальций | — | 0,98 | — | — | — |
| Кобальт | — | 0,69 | — | — | — |
| Литий | — | 0,71 | 0,73 | — | — |
| Магний | 1,6 | 1,5 | 1,5 | 1,45 | — |
| Медь | 4,05 | 3,85 | 3,82 | 3,76 | 3,50 |
| Молибден | 1,4 | 1,43 | — | — | 1,04 (1000°) |
| Натрий | 1,35 | 1,35 | 0,85 | 0,76 | 0,60 |
| Никель | 0,97 | 0,91 | 0,83 | 0,64 | 0,66 |
| Ниобий | 0,49 | 0,49 | 0,51 | 0,56 | — |
| Олово | 0,74 | 0,64 | 0,60 | 0,33 | — |
| Палладий | 0,69 | 0,67 | 0,74 | — | — |
| Платина | 0,68 | 0,69 | 0,72 | 0,76 | 0,84 |
| Рений | — | 0,71 | — | — | — |
| Родий | 1,54 | 1,52 | 1,47 | — | — |
| Ртуть | 0,33 | 0,09 | 0.1 | 0,115 | — |
| Свинец | 0,37 | 0,35 | 0,335 | 0,315 | 0,19 |
| Серебро | 4,22 | 4,18 | 4,17 | 3,62 | — |
| Сурьма | 0,23 | 0,18 | 0,17 | 0,17 | 0,21 |
| Таллий | 0,41 | 0,43 | 0,49 | 0,25 (400 0) | |
| Тантал | 0,54 | 0,54 | — | — | — |
| Титан | — | — | 0,16 | 0,15 | — |
| Торий | — | 0,41 | 0,39 | 0,40 | 0,45 |
| Уран | — | 0,24 | 0,26 | 0,31 | 0,40 |
| Хром | — | 0,86 | 0,85 | 0,80 | 0,63 |
| Цинк | 1,14 | 1,13 | 1,09 | 1,00 | 0,56 |
| Цирконий | — | 0,21 | 0,20 | 0,19 | — |
Значение для человека
Хром присутствует в организме человека изначально.
Здоровье
Он – участник ряда биологических процессов:
- Липидный, углеродный обмен.
- Выведение «плохого» холестерина
- Баланс сахара в крови.
- Укрепление костной ткани.
- Активация действия инсулина.
- Способность замещать йод.
- Стимуляция регенерации тканей.
Достаточное содержание хрома в организме критично важно для людей с лишним весом, диабетом, заболеваниями щитовидной железы, сердца, сосудов.
Питание
Хромом богаты продукты всех основных групп:
- Мясо – курятина, говядина (и печень);
- Рыба – скумбрия, тунец, сельдь.
- Крупы – манная, перловая.
- Овощи – помидоры, редис, зеленый лук.
Металлом насыщены сыры, бобовые, кукурузное масло, фрукты, хлеб из муки крупного помола, пивные дрожжи.
Дозировка
Ежесуточная потребность в хроме (мкг):
- Дети – 12-34 (в зависимости от возраста).
- Женщины – 55-68.
- Мужчины – 59-79.
При беременности у женщин, активном образе жизни, физических нагрузках у мужчин потребность удваивается.
Общие сведения:
| 100 | Общие сведения | |
| 101 | Название | Хром |
| 102 | Прежнее название | |
| 103 | Латинское название | Chromium |
| 104 | Английское название | Chromium |
| 105 | Символ | Cr |
| 106 | Атомный номер (номер в таблице) | 24 |
| 107 | Тип | Металл |
| 108 | Группа | Амфотерный, переходный, чёрный металл |
| 109 | Открыт | Луи-Николя Воклен, Франция, 1797 г. |
| 110 | Год открытия | 1797 г. |
| 111 | Внешний вид и пр. | Твёрдый металл голубовато-белого цвета |
| 112 | Происхождение | Природный материал |
| 113 | Модификации | |
| 114 | Аллотропные модификации | |
| 115 | Температура и иные условия перехода аллотропных модификаций друг в друга | |
| 116 | Конденсат Бозе-Эйнштейна | 52Cr |
| 117 | Двумерные материалы | |
| 118 | Содержание в атмосфере и воздухе (по массе) | 0 % |
| 119 | Содержание в земной коре (по массе) | 0,014 % |
| 120 | Содержание в морях и океанах (по массе) | 6,0·10-8 % |
| 121 | Содержание во Вселенной и космосе (по массе) | 0,0015 % |
| 122 | Содержание в Солнце (по массе) | 0,002 % |
| 123 | Содержание в метеоритах (по массе) | 0,3 % |
| 124 | Содержание в организме человека (по массе) | 3,0·10-6 % |
Применение
Металлический хром очень стоек к окислению на воздухе, так как его поверхность покрыта тончайшей и плотной плёнкой из оксидов, которая препятствует коррозии. При этом, будучи дополнительно пассивированным реакцией с концентрированными кислотами, хром становится чрезвычайно коррозионно устойчивым материалом, который можно использовать для покрытия металлических изделий (хромирования).
Автомобиль BMW M3, покрытый блестящим слоем хрома
Удельная теплоемкость цветных сплавов
В таблице приведены величины удельной (массовой) теплоемкости двухкомпонентных и многокомпонентных цветных сплавов, не содержащих железа, при температуре от 123 до 1000К. Теплоемкость указана в размерности кДж/(кг·град). Дана теплоемкость следующих сплавов: сплавы, содержащие алюминий, медь, магний, ванадий, цинк, висмут, золото, свинец, олово, кадмий, никель, иридий, платина, калий, натрий, марганец, титан, сплав висмут — свинец — олово, сплав висмут-свинец, висмут — свинец — кадмий, алюмель, сплав липовица, нихром, сплав розе.
Также существует отдельная таблица, где представлена удельная теплоемкость металлов при различных температурах.