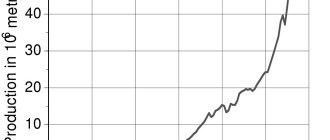
Оксиды — широко распространённый в природе тип соединений, который можно наблюдать даже в повседневной жизни, в быту. Примером могут служить песок, вода, ржавчина, известь, углекислый газ, ряд природных красителей. Руда многих ценных металлов по своей природе является оксидом, вследствие чего представляет большой интерес для научных и производственных исследований.
Соединение химических элементов с кислородом называют оксидами. Как правило, образуются они при накаливании каких-либо веществ на воздухе. Различают кислотные и основные оксиды. Металлы образуют основные оксиды, в то время как неметаллы — кислотные. За исключением оксидов хрома и марганца, которые также являются кислотными. В данной статье рассматривается представитель основных оксидов — CuO (II).
Краткая характеристика оксида меди (II):
Оксид меди (II) – неорганическое вещество черного цвета.
Так как валентность меди меняется и равна одному, двум или трем, то оксид меди содержит соответственно два атома меди и один атом кислорода, один атом меди и один атом кислорода, два атома меди и три атома кислорода.
Оксид двухвалентной меди содержит соответственно один атом меди и один атом кислорода.
Химическая формула оксида меди (II) CuO.
Порошок. Не растворяется в воде.
Химическая формула: CuO
Молекула его состоит из атома Cu с молекулярной массой 64 а. е. м. и атома O, молекулярная масса 16 а. е. м., где а. е. м. — атомная единица массы, она же дальтон, 1 а. е. м. = 1,660 540 2(10) × 10−27 кг = 1,660 540 2(10) × 10–24 г. Соответственно молекулярная масса соединения равняется: 64 + 16 = 80 а. е. м.
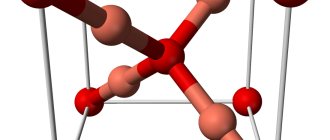
Кристаллическая решётка: моноклинная сингония. Что обозначает такой тип осей симметрии кристалла, когда две оси пересекаются под косым углом и имеют различную длину, а третья ось расположена по отношению к ним под углом 90°.
Плотность 6,51 г/см3. Для сопоставления, плотность чистого золота равна 19,32 г/см³, а плотность поваренной соли составляет 2,16 г /см 3.
Плавится при температуре 1447 °C, под давлением кислорода.
Разлагается при накаливании до 1100 °C и преобразуется в оксид меди (I):
4CuO = 2Cu2O + O 2.
С водой не реагирует и не растворяется в ней.
Зато вступает в реакцию с водным раствором аммиака, с образованием гидроксида тетраамминмеди (II): CuO + 4NH3 + H2O = [Cu (NH3)4](OH) 2.
В кислотной среде образует сульфат и воду: CuO + H2SO4 = CuSO4 + H2O.
Реагируя со щёлочью, создаёт купрат: CuO + 2 NaOH → Na2CuO2 + H2O.
Физические свойства оксида меди (II):
| Наименование параметра: | Значение: |
| Химическая формула | CuO |
| Синонимы и названия иностранном языке | меди окись (устар. рус.) сopper (II) oxide (англ.) тенорит (рус.) |
| Тип вещества | неорганическое |
| Внешний вид | черный порошок |
| Цвет | черный |
| Вкус | —* |
| Запах | — |
| Агрегатное состояние (при 20 °C и атмосферном давлении 1 атм.) | твердое вещество |
| Плотность (состояние вещества – твердое вещество, при 20 °C), кг/м3 | 6310 |
| Плотность (состояние вещества – твердое вещество, при 20 °C), г/см3 | 6,31 |
| Температура кипения, °C | 2000 |
| Температура плавления, °C | 1447 |
| Температура разложения, °C | 800 |
| Молярная масса, г/моль | 79,545 |
* Примечание:
— нет данных.
Опыт 2. Определение углерода и водорода сожжением вещества с оксидом меди (II)
Реактивы и материалы: глюкоза (или глицерин, крахмал, сахар); оксид меди (порошок); баритовая вода, насыщенный водный раствор; сульфат меди (II) безводный. Оборудование: газоотводная трубка с пробкой; стеклянная палочка; микролопатка.
В сухую пробирку 1(рис. насыпают черный порошок оксида меди (слой высотой около 5 мм). Добавляют половину микролопатки глюкозы и тщательно перемешивают, встряхивая пробирку. В верхнюю часть пробирки помещают небольшой комочек ваты, на который насыпают немного белого порошка безводного сульфата меди (II). Пробирку закрывают пробкой с газоотводной трубкой. При этом конец трубки должен почти упираться в вату с CuSО4.
Нижний конец трубки опускают в пробирку 2,
предварительно налив в нее 5-6 капель баритовой (или известковой) воды. Пробирку 1нагревают на пламени
горелки.
Через несколько секунд из газоотводной трубки начинают выходить пузырьки газа, и баритовая вода мутнеет вследствие выделения белого осадка углекислого бария. Пробирку 2удаляют. Продолжают нагревать пробирку 1,
пока пары воды не достигнут белого порошка обезвоженного медного купороса, находящегося на ватной пробке, и не вызовут изменения его окраски вследствие образования кристаллогидрата CuSO4*5H2O .
Химизм процесса:
C6H12O6 + 12CuO → 6CO2 + 6H2O + 12Cu
CO2 + Ba(OH)2 → BaCO3 + H2O
CuSO4 + 5H2O → CuSO4*5H2O
Метод основан на том, что при прокаливании органического вещества в смеси с окислителем (СuО) происходит окисление углерода органического вещества в диоксид углерода, а водорода – в воду. Оксид меди при этом восстанавливается до металлической меди.
Выделение диоксида углерода доказывается появлением белого осадка углекислого бария. Воду в продуктах сжигания обнаруживают по образованию синих кристаллов медного купороса.
Реактивы и материалы: глюкоза (или глицерин, крахмал, сахар); оксид меди (порошок); баритовая вода, насыщенный водный раствор; сульфат меди (II) безводный. Оборудование: газоотводная трубка с пробкой; стеклянная палочка; микролопатка.
В сухую пробирку 1(рис. насыпают черный порошок оксида меди (слой высотой около 5 мм). Добавляют половину микролопатки глюкозы и тщательно перемешивают, встряхивая пробирку. В верхнюю часть пробирки помещают небольшой комочек ваты, на который насыпают немного белого порошка безводного сульфата меди (II). Пробирку закрывают пробкой с газоотводной трубкой. При этом конец трубки должен почти упираться в вату с CuSО4.
Нижний конец трубки опускают в пробирку 2,
предварительно налив в нее 5-6 капель баритовой (или известковой) воды. Пробирку 1нагревают на пламени
горелки.
Через несколько секунд из газоотводной трубки начинают выходить пузырьки газа, и баритовая вода мутнеет вследствие выделения белого осадка углекислого бария. Пробирку 2удаляют. Продолжают нагревать пробирку 1,
пока пары воды не достигнут белого порошка обезвоженного медного купороса, находящегося на ватной пробке, и не вызовут изменения его окраски вследствие образования кристаллогидрата CuSO4*5H2O .
Химизм процесса:
C6H12O6 + 12CuO → 6CO2 + 6H2O + 12Cu
CO2 + Ba(OH)2 → BaCO3 + H2O
CuSO4 + 5H2O → CuSO4*5H2O
Метод основан на том, что при прокаливании органического вещества в смеси с окислителем (СuО) происходит окисление углерода органического вещества в диоксид углерода, а водорода – в воду. Оксид меди при этом восстанавливается до металлической меди.
Выделение диоксида углерода доказывается появлением белого осадка углекислого бария. Воду в продуктах сжигания обнаруживают по образованию синих кристаллов медного купороса.
Получение оксида меди (II):
Оксид меди (II) получается в результате следующих химических реакций:
1. окисления меди:
2Cu + O2 → CaО.
2. термического разложения гидроксида меди (II), нитрата меди (II), карбоната меди (II):
Cu(OH)2 → CuО + H2O (to);
2Cu(NO3)2 → 2CuО + 4NO2 + O2 (to);
CuCO3 → CuО + CO2 (to).
3. нагревания малахита:
Cu2CO3(OH)2 → 2CuО + CO2 + H2O (to).
Реакция CuO NaOH
Образуется:
- путём прокаливания гидроксида меди (II) при температуре 200 °C: Cu(OH)2 = CuO + H2O;
- при окислении металлической меди на воздухе при температуре 400–500 °C: 2Cu + O2 = 2CuO;
- при высокотемпературной обработке малахита: (CuOH)₂CO₃ —> 2CuO + CO₂ + H₂O.
Восстанавливается до металлической меди —
- в реакции с водородом: CuO + H2 = Cu + H2O;
- с угарным газом (монооксид углерода): CuO + CO = Cu + CO2;
- с активным металлом: CuO + Mg = Cu + MgO.
Токсичен. По степени неблагоприятного воздействия на человеческий организм причисляется к веществам второго класса опасности. Вызывает раздражение слизистых оболочек глаз, кожных покровов, дыхательных путей и желудочно-кишечной системы. При взаимодействии с ним обязательно использование таких средств защиты, как резиновые перчатки, респираторы, защитные очки, спецодежду.
Вещество взрывоопасно и легко воспламеняется.
Применяется в промышленности, как минеральная составляющая комбикормов, в пиротехнике, при получении катализаторов химических реакций, как красящий пигмент для стекла, эмалей, керамики.
Окислительные свойства оксида меди (II) наиболее часто применяются в лабораторных исследованиях, когда необходим элементарный анализ, связанный с изучением органических материалов на предмет наличия в них водорода и углерода.
Немаловажно, что CuO (II) достаточно широко распространён в природе, как минерал тенерит, другими словами — это природное соединение руды, из которого можно получить медь.
Латинское наименование Cuprum и соответствующий ему символ Cu происходит от названия острова Кипр. Именно оттуда, через Средиземное море вывозили этот ценный металл древние римляне и греки.
Медь входит в число семи наиболее распространённых в мире металлов и состоит на службе у человека с древних времён. Однако в первозданном, металлическом состоянии встречается довольно редко. Это мягкий, легко поддающийся обработке металл, отличающийся высокой плотностью, очень качественный проводник тока и тепла. По электрической проводимости уступает только серебру, в то время как является более дешёвым материалом. Широко используется в виде проволоки и тонкого листового проката.
Химические соединения меди отличаются повышенной биологической активностью. В животных и растительных организмах они участвуют в процессах синтеза хлорофилла, поэтому считаются очень ценным компонентом в составе минеральных удобрений.
Необходима медь и в рационе человека. Недостаток её в организме может привести к различным заболеваниям крови.
Химические свойства оксида меди (II). Химические реакции оксида меди (II):
Оксид меди (II) относится к основным оксидам.
Химические свойства оксида меди (II) аналогичны свойствам основных оксидов других металлов. Поэтому для него характерны следующие химические реакции:
1. реакция оксида меди (II) с водородом:
CuО + H2 → Cu + H2О (t = 300 oC).
В результате реакции образуется медь и вода.
2. реакция оксида меди (II) с углеродом:
CuО + С → Cu + СО (t = 1200 oC).
В результате реакции образуется медь и оксид углерода.
3. реакция оксида меди (II) с серой:
CuО + 2S → Cu + S2О (t = 150-200 oC).
Реакция протекает в вакууме. В результате реакции образуется медь и оксид серы.
4. реакция оксида меди (II) с алюминием:
3CuО + 2Al → 3Cu + Al2О3 (t = 1000-1100 oC).
В результате реакции образуется медь и оксид алюминия.
5. реакция оксида меди (II) с медью:
CuО + Cu → Cu2О (t = 1000-1200 oC).
В результате реакции образуется оксид меди (I).
6. реакция оксида меди (II) с оксидом лития:
CuО + Li2О → Li2CuО2 (t = 800-1000 oC, О2).
Реакция протекает в токе кислорода. В результате реакции образуется купрат лития.
7. реакция оксида меди (II) с оксидом натрия:
CuО + Na2О → Na2CuО2 (t = 800-1000 oC, О2).
Реакция протекает в токе кислорода. В результате реакции образуется купрат натрия.
8. реакция оксида меди (II) с оксидом углерода:
CuО + СО → Cu + СО2.
В результате реакции образуется медь и оксид углерода (углекислый газ).
9. реакция оксида меди (II) с оксидом железа:
CuО + Fe2O3 → CuFe2О4 (to).
В результате реакции образуется соль – феррит меди. Реакция протекает при прокаливании реакционной смеси.
10. реакция оксида меди (II) с плавиковой кислотой:
CuO + 2HF → CuF2 + H2O.
В результате химической реакции получается соль – фторид меди и вода.
11. реакция оксида меди (II) с азотной кислотой:
CuO + 2HNO3 → 2Cu(NO3)2 + H2O.
В результате химической реакции получается соль – нитрат меди и вода.
Аналогично проходят реакции оксида меди (II) и с другими кислотами.
12. реакция оксида меди (II) с бромистым водородом (бромоводородом):
CuO + 2HBr → CuBr2 + H2O.
В результате химической реакции получается соль – бромид меди и вода.
13. реакция оксида меди (II) с йодоводородом:
CuO + 2HI → CuI2 + H2O.
В результате химической реакции получается соль – йодид меди и вода.
14. реакция оксида меди (II) с гидроксидом натрия:
CuO + 2NaOH → Na2CuO2 + H2O.
В результате химической реакции получается соль – купрат натрия и вода.
15. реакция оксида меди (II) с гидроксидом калия:
CuO + 2KOH → K2CuO2 + H2O.
В результате химической реакции получается соль – купрат калия и вода.
16. реакция оксида меди (II) с гидроксидом натрия и водой:
CuO + 2NaOH + H2O → Na2[Cu2(OН)]2 (t = 100 oC).
Гидрокосид натрия растворен в воде. Раствор гидроксида натрия в воде 20-30 %. Реакция протекает при киппении. В результате химической реакции получается тетрагидроксокупрат натрия.
17. реакция оксида меди (II) с надпероксидом калия:
2CuO + 2KO2 → 2KCuO2 + О2 (t = 400-500 oC).
В результате химической реакции получается соль – купрат (III) калия и кислород.
18. реакция оксида меди (II) с пероксидом калия:
2CuO + 2K2O2 → 2KCuO2 (t = 700 oC).
В результате химической реакции получается соль – купрат (III) калия.
19. реакция оксида меди (II) с пероксидом натрия:
2CuO + 2Na2O2 → 2NaCuO2 (t = 700 oC).
В результате химической реакции получается соль – купрат (III) натрия.
20. реакция оксида меди (II) с аммиаком:
3CuO + 2NH3 → N2 + 3Cu + 3H2O (t = 500-550 oC).
Аммиак пропускают через нагретый оксид меди (II). В результате химической реакции получается азот, медь и вода.
6CuO + 4NH3 → 2Cu3N + N2 + 6H2O (t = 250-300 oC).
В результате химической реакции получается нитрид меди, азот и вода.
21. реакция оксида меди (II) и йодида алюминия:
6CuO + 4AlI3 → 6CuI + 2Al2O3 + 3I2 (t = 230 oC).
В результате химической реакции получаются соль – йодид меди, оксид алюминия и йод.
Оксид меди (I, II, III): свойства, получение, применение
Как вам известно, в химии существует четыре класса неорганических соединений. Веществ, представляющих каждый из них, очень много, но лидирующее положение, несомненно, занимают оксиды. У одного химического элемента может быть сразу несколько разных бинарных соединений с кислородом. Такое свойство имеет и медь. У нее существует три оксида. Давайте рассмотрим их детальнее.
Оксид меди (I)
Его формула — Cu2O. В некоторых источниках данное соединение могут называть гемиоксидом меди, оксидом димеди или закисью меди.
Свойства
Является кристаллическим веществом, имеющим коричнево-красный цвет. Этот оксид не растворяется в воде и этиловом спирте. Может плавиться, не разлагаясь, при температуре чуть больше 1240оС. Данное вещество не взаимодействует с водой, но может переводиться в раствор, если участниками реакции с ним будут концентрированные хлоровородная кислота, щелочь, азотная кислота, гидрат аммиака, соли аммония, серная кислота.
Получение оксида меди (I)
Его можно получить, нагрев металлическую медь, или в такой среде, где кислород имеет малую концентрацию, а также в токе некоторых оксидов азота и вместе с оксидом меди (II). Кроме того, он может стать продуктом реакции термического разложения последнего. Оксид меди (I) получится и в том случае, если нагреть сульфид меди (I) в токе кислорода. Есть и другие, более сложные способы его получения (например, восстановление одного из гидроксидов меди, ионный обмен любой соли одновалентной меди с щелочью и т.п.), но их практикуют только в лабораториях.
Применение
Нужен в качестве пигмента, когда окрашивают керамику, стекло; компонента красок, которые защищают подводную часть судна от обрастания. Используется также как фунгицид. Без него не обходятся и меднозакисные вентили.
Оксид меди (II)
Его формула — CuO. Во многих источниках может встречаться под названием окиси меди.
Свойства
Это высший оксид меди. Вещество имеет вид черных кристаллов, которые почти не растворяются в воде. Взаимодействует с кислотой и при этой реакции образует соответствующую соль двухвалентной меди, а также воду. При его сплавлении с щелочью продукты реакции представлены купратами. Разложение оксида меди (II) происходит при температуре около 1100оС. Аммиак, монооксид углерода, водород и уголь способны извлекать из этого соединения металлическую медь.
Получение
Его можно получить при нагревании металлической меди в воздушной среде при одном условии — температура нагревания должна быть ниже 1100оС. Также оксид меди (II) может получиться, если нагреть карбонат, нитрат, двухвалентный гидроксид меди.
Применение
С помощью данного оксида окрашивают в зеленый или синий цвет эмаль и стекло, а также производят медно-рубиновую разновидность последнего. В лаборатории этим оксидом обнаруживают восстановительные свойства веществ.
Оксид меди (III)
Его формула — Cu2O3. Имеет традиционное название, которое звучит, наверное, немного необычно — окисел медь.
Свойства
Имеет вид красных кристаллов, не растворяющихся в воде. Разложение этого вещества происходит при температуре 400оС, продукты данной реакции — оксид меди (II) и кислород.
Получение
Его можно получить, окисляя двухвалентный гидроксид меди с помощью пероксидисульфата калия. Необходимое условие реакции — щелочная среда, в которой она должна происходить.
Применение
Данное вещество само по себе не используется. В науке и промышленности более широкое распространение находят продукты его разложения — оксид меди (II) и кислород.
Заключение
Вот и все оксиды меди. Их несколько из-за того, что медь имеет переменную валентность. Существуют и другие элементы, у которых есть по несколько оксидов, но о них поговорим в другой раз.
Кристаллические решётка:
| 300 | Кристаллическая решётка |
| 311 | Кристаллическая решётка #1 |
| 312 | Структура решётки |
| 313 | Параметры решётки |
| 314 | Отношение c/a |
| 315 | Температура Дебая |
| 316 | Название пространственной группы симметрии |
| 317 | Номер пространственной группы симметрии |